پتاسیم نیترات (Potassium Nitrate)
پتاسیم نیترات (Potassium Nitrate)پتاسیم نیترات (Potassium Nitrate)
پتاسیم نیترات (Potassium Nitrate)ساختار مولکول سیکلوهگزان
مولکول سیکلوهگزان
سیکلوهگزان سیکلوآکلان با فرمول مولکولی C6H12 است. سیکلوهگزان به عنوان حلال غیر قطبی برای صنایع شیمیایی و همچنین به عنوان ماده اولیه برای تولید صنعتی اسید آدیپیک و کاپرولاکتام مورد استفاده قرار می گیرد که هر دوی آنها واسطه های مورد استفاده در تولید نایلون هستند. در مقیاس صنعتی ، سیکلوهگزان با واکنش بنزن با هیدروژن تولید می شود. سیکلو هگزان به دلیل ویژگی های شیمیایی و تطبیقی منحصر به فرد خود در آزمایشگاه ها در تجزیه و تحلیل و به عنوان استاندارد استفاده می شود.
مولکول سیکلو هگزان با استفاده از Jsmol مراجعه کنید - برای ساختارهای سه بعدی
ساختار مولکول سیکلوهگزان
حلقه 6 راس با شکل یک شش ضلعی کامل مطابقت ندارد. شکل شش ضلعی مسطح مسطح دارای زاویه قابل توجهی است زیرا پیوندهای آن 109.5 درجه نیستند. فشار پیچشی نیز به دلیل همه پیوندهای گرفتگی شده قابل توجه خواهد بود. بنابراین ، برای کاهش فشار پیچشی ، سیکلوهگزان از یک ساختار سه بعدی استفاده می کند که به عنوان ترکیب صندلی شناخته می شود. ترکیب جدید ، کربن ها را در زاویه 109.5 درجه سانتی گراد قرار می دهد. نیمی از هیدروژن ها در صفحه حلقه (استوایی) و نیمی دیگر عمود بر صفحه (محوری) هستند. این ترکیب باعث ایجاد پایدارترین ساختار سیکلوهگزان می شود. ترکیب دیگری از سیکلوهگزان وجود دارد ، که به شکل قایق معروف است ، اما به شکل صندلی کمی پایدارتر تبدیل می شود. اگر سیکلوهگزان با یک جایگزین بزرگ تک جایگزین شود ، به احتمال زیاد جایگزین در موقعیت استوایی متصل می شود ، زیرا این ترکیب کمی پایدارتر است.
سیکلو هگزان دارای کمترین زاویه و کرنش پیچشی در بین همه سیکلوآکلان ها است ، در نتیجه سیکلو هگزان در کرنش حلقه کل 0 ، ترکیبی از زاویه و کرنش پیچشی در نظر گرفته شده است. این امر همچنین باعث می شود سیکلوهگزان پایدارترین سیکلوآلکان ها باشد و بنابراین در مقایسه با سایر سیکلوآلکانها کمترین میزان حرارت را در هنگام سوزاندن تولید می کند.
موقعیت صندلی سیکلوهگزان
یک مولکول سیکلوهگزان در شکل بندی اتمهای هیدروژن در موقعیتهای محوری با رنگ قرمز نشان داده می شوند ، در حالی که آنهایی که در موقعیت استوایی قرار دارند به رنگ آبی هستند.
واکنش با سیکلوهگزان
سیکلوهگزان خالص به خودی خود نسبتاً غیرفعال است ، زیرا یک هیدروکربن غیر قطبی و آبگریز است. این می تواند با اسیدهای بسیار قوی مانند سیستم فوق اسیدی HF + SbF5 واکنش دهد که باعث پروتوناسیون اجباری و "ترک خوردن هیدروکربن" می شود. سیکلو هگزان های جایگزین ، با این حال ، ممکن است تحت شرایط مختلف ، که بسیاری از آنها برای شیمی آلی مهم هستند ، واکنش پذیر باشند. سیکلوهگزان بسیار قابل اشتعال است.
کاربردها و خواص سیکلوهگزان را در لینک زیر بخوانید
https://bismoot.com/blog/%d8%b3%db%8c%da%a9%d9%84%d9%88%d9%87%da%af%d8%b2%d8%a7%d9%86/
مشتقات سیکلوهگزان
ترتیب خاص گروههای عملکردی در مشتقات سیکلوهگزان و در واقع در بیشتر مولکولهای سیکلوآلکان ، در واکنشهای شیمیایی ، به ویژه واکنشهای مربوط به نوکلئوفیلها ، بسیار مهم است. جایگزین های حلقه باید در شکل محوری باشند تا با سایر مولکول ها واکنش نشان دهند. به عنوان مثال ، واکنش بروموسیکلوهگزان و یک نوکلوفیل معمولی ، یک آنیون هیدروکسید ، منجر به سیکلوهگزن می شود.
این واکنش ، که معمولاً به عنوان واکنش حذف یا دالوژناسیون (به ویژه E2) شناخته می شود ، مستلزم آن است که جایگزین برم در تشکیل محوری باشد و با اتم H محوری دیگر واکنش نشان دهد. با فرض اینکه بروموسیکلو هگزان در تشکیل مناسب برای واکنش قرار داشته باشد ، واکنش E2 به شرح زیر شروع می شود:
پیوند زوج الکترونی بین C-Br به Br منتقل می شود و Br∠را تشکیل می دهد و آن را از سیکلوهگزان آزاد می کند.
nucleophile (-OH) یک جفت الکترون به H محوری مجاور می دهد ، H را آزاد می کند و به آن متصل می شود تا H2O ایجاد شود
پیوند جفت الکترون بین H محوری مجاور به پیوند بین دو C-C حرکت می کند و C = C را ایجاد می کند
توجه: هر سه مرحله به طور همزمان اتفاق می افتد ، مشخصه همه واکنش های E2.
واکنش فوق بیشتر واکنش E2 ایجاد می کند و در نتیجه محصول بیشتر (~ 70)) سیکلوهگزن خواهد بود. با این حال ، درصد با شرایط متفاوت است و به طور کلی ، دو واکنش متفاوت (E2 و Sn2) با هم رقابت می کنند. در واکنش فوق ، یک واکنش Sn2 به جای گروه برم ، گروه هیدروکسیل (OH-) را جایگزین می کند ، اما یک بار دیگر ، Br باید محوری باشد تا واکنش نشان دهد. هنگامی که جایگزینی SN2 کامل شد ، گروه جدید جایگزین OH به سرعت به موقعیت استوایی پایدارتر برمی گردد (mill 1 میلی ثانیه).
از نظر تجاری بیشتر سیکلوهگزان تولید شده با اکسیداسیون کاتالیزوری به مخلوط سیکلوهزانون-سیکلوهگزانول تبدیل می شود. سپس روغن KA به عنوان ماده اولیه اسید آدیپیک و کاپرولاکتام استفاده می شود. عملاً ، اگر محتوای سیکلو هگزانول روغن KA بیشتر از سیکلو هگزانون باشد ، به احتمال زیاد (مقرون به صرفه) به اسید آدیپیک تبدیل می شود و در حالت معکوس ، احتمال تولید کاپرولاکتام بیشتر است. چنین نسبت در روغن KA را می توان با انتخاب کاتالیزهای اکسیداسیون مناسب کنترل کرد. مقداری از سیکلوهگزان به عنوان حلال آلی استفاده می شود.

سیکلو هگزان در تحقیقات
اگرچه در مورد این هیدروکربن چرخه ای اطلاعات زیادی در دست است ، تحقیقات انجام دهیدقوس هنوز روی سیکلو هگزان و بنزن و سیکلو هگزان فاز جامد برای تعیین بازده هیدروژن مخلوط در هنگام تابش در دمای 195 درجه سانتی گراد انجام می شود.
تاریخ
بر خلاف ترکیباتی مانند بنزن ، سیکلوهگزان را نمی توان به راحتی از منابع طبیعی مانند زغال سنگ بدست آورد. در اواخر قرن نوزدهم ، محققان شیمی اولیه باید به سنتز آلی وابسته بودند. آنها 30 سال طول کشید تا جزئیات را بررسی کنند [1]. در سال 1867 مارسلین برتلوت در دمای بالا بنزن را با اسید هیدروودیک کاهش داد. او نه تنها به دلیل مطابقت مناسب در نقطه جوش (69 درجه سانتی گراد) ، بلکه به دلیل اینکه بنزن یک مولکول چرخه ای (مانند آگوست ککوله معاصر خود) نیست ، بلکه واکنش را بعنوان یک هگزان به عنوان ن هگزان تشخیص داد. از استیلن در سال 1870 یکی از شکاکانش آدولف فون بایر واکنش را تکرار کرد و همان محصول واکنش را هگزاهیدروبنزن بیان کرد و در سال 1890 ولادیمیر مارکوفنیکوف معتقد بود که قادر است همان ترکیب را از نفت قفقاز تقطیر کند که معجون خود را هگزانفتن نامیده است.
در 1894 بایر سیکلو هگزان را با تراکم دیکمن اسید پیملیک سنتز کرد و به دنبال آن چندین بار کاهش یافت. و در همان سال E. Haworth و W.H. پرکین جونیور (1860 - 1929) همین کار را در واکنش وورتز با 1،6 -دیبروموگزان انجام داد. به طور شگفت انگیزی سیکلو هگزان های آنها 10 درجه سانتیگراد بیشتر از هگزاهیدروبنزن یا هگزانفتن جوشید اما این معما در سال 1895 توسط مارکوفنیکوف ، نیومنات کیشنر و نیکولای حل شد. زلینسکی هنگامی که هگزاهیدروبنزن و هگزانفتن را مجدداً متیل سیکلوپنتان تشخیص دادند ، نتیجه یک واکنش بازآرایی غیرمنتظره بود.
منبع
کربن اکتیو چیست؟+ خرید اکربن اکتیو
کربن اکتیو چیست؟
کربن اکتیو
کربن فعال ، که زغال فعال نیز نامیده می شود ، شکلی از کربن است که دارای منافذ کوچک و کم حجم است و سطح آن را افزایش می دهد که برای جذب یا واکنش های شیمیایی در دسترس است. گاهی اوقات فعال با اکتیو جایگزین می شود.
یک گرم کربن فعال به دلیل میزان بالای ریزخلاری ، دارای مساحت بیش از 3000 متر مربع (32000 فوت فوت مربع) است که توسط جذب گاز تعیین می شود. سطح فعال سازی کافی برای کاربرد مفید را می توان تنها از سطح زیاد بدست آورد. تصفیه شیمیایی بیشتر اغلب ویژگی های جذب را افزایش می دهد.
کربن فعال معمولاً از زغال چوب مشتق می شود. وقتی از زغال سنگ مشتق می شود به آن زغال فعال گفته می شود. کک فعال از کک مشتق شده است.
جهت خرید کربن اکتیو به لینک زیر بروید.
https://bismoot.com/blog/%da%a9%d8%b1%d8%a8%d9%86-%d8%a7%da%a9%d8%aa%db%8c%d9%88/
استفاده می کند
کربن فعال در ذخیره متان و هیدروژن ، تصفیه هوا ، بازیابی حلال ، بدون کافئین ، تصفیه طلا ، استخراج فلزات ، تصفیه آب ، دارو ، تصفیه فاضلاب ، فیلترهای هوا در دستگاه های تنفس ، فیلترهای در هوای فشرده ، سفید کردن دندان ها استفاده می شود. ، تولید کلرید هیدروژن و بسیاری از کاربردهای دیگر.
صنعتی
یکی از کاربردهای مهم صنعتی شامل استفاده از کربن فعال در تکمیل فلزات برای تصفیه محلول های آبکاری است. به عنوان مثال ، این تکنیک اصلی تصفیه برای حذف ناخالصی های آلی از محلول های نیکل آبکاری روشن است. انواع مواد شیمیایی آلی برای بهبود کیفیت رسوب و افزایش خواص مانند روشنایی ، نرمی ، شکل پذیری و غیره به محلول های آبکاری اضافه می شوند. به دلیل عبور جریان مستقیم و واکنش های الکترولیتی اکسیداسیون آندی و کاهش کاتدی ، افزودنی های آلی محصولات تجزیه ناخواسته تولید می کنند. در محلول تجمع بیش از حد آنها می تواند بر کیفیت آبکاری و خواص فیزیکی فلز رسوب شده تأثیر منفی بگذارد. تصفیه کربن فعال چنین ناخالصی هایی را حذف کرده و عملکرد آبکاری را به سطح دلخواه باز می گرداند.
پزشکی
مقاله اصلی: زغال فعال (دارویی)
زغال فعال برای مصارف پزشکی
کربن فعال برای درمان مسمومیت ها و مصرف بیش از حد بدن پس از مصرف خوراکی استفاده می شود. قرص ها یا کپسول های کربن فعال در بسیاری از کشورها به عنوان دارویی بدون نسخه برای درمان اسهال ، سوء هاضمه و نفخ استفاده می شوند. با این حال ، زغال فعال هیچ تاثیری بر گاز روده و اسهال نشان نمی دهد و معمولاً در صورت مسمومیت ناشی از خوردن مواد خورنده ، اسید بوریک ، فرآورده های نفتی ، از نظر پزشکی بی اثر است و به ویژه در برابر مسمومیت اسیدهای قوی یا قلیایی ، سیانید ، آهن بی اثر است. ، لیتیوم ، آرسنیک ، متانول ، اتانول یا اتیلن گلیکول. [6] کربن فعال مانع از جذب این مواد شیمیایی در بدن انسان نمی شود. این دارو در فهرست داروهای ضروری سازمان بهداشت جهانی ، ایمن ترین و م effectiveثرترین داروهای مورد نیاز در یک سیستم بهداشتی قرار دارد.
استفاده نادرست (به عنوان مثال در ریه ها) منجر به آسپیراسیون ریوی می شود که در صورت عدم شروع درمان فوری گاهی اوقات می تواند کشنده باشد.
شیمی تجزیه
کربن فعال ، در ترکیب 50٪ وزنی/وزنی با celite ، به عنوان فاز ساکن در جداسازی کروماتوگرافی کم فشار کربوهیدراتها (مونو ، دی ، تری ساکاریدها) با استفاده از محلولهای اتانول (5 تا 50٪) به عنوان فاز متحرک در پروتکل های تحلیلی یا مقدماتی
کربن فعال برای استخراج ضد انعقاد مستقیم خوراکی (DOAC) مانند دبیگاتران ، آپیکسان ، ریواروکسابان و ادوکسابان از نمونه های پلاسمای خون مفید است. برای این منظور از آن "minitablets" ساخته شده است ، هر کدام حاوی 5 میلی گرم کربن فعال برای درمان 1 میلی لیتر نمونه DOAC است. از آنجا که این کربن فعال هیچ تاثیری بر عوامل انعقاد خون ندارد ، هپارین یا اکثر داروهای ضد انعقاد دیگر این امر باعث می شود نمونه پلاسما از نظر ناهنجاری هایی که در غیر این صورت تحت تأثیر DOAC قرار می گیرند ، مورد تجزیه و تحلیل قرار گیرد.
منبع
دی اتانول آمین در لوازم آرایشی+ خرید دی اتانول آمین
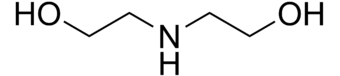
دی اتانول آمین
مصرف کنندگان و تولیدکنندگان ممکن است در مورد ایمنی دی اتانول آمین (DEA) و ترکیبات مرتبط در لوازم آرایشی سوال داشته باشند. اطلاعات زیر از برنامه ملی سم شناسی (NTP) و FDA است.
NTP در سال 1998 مطالعه ای را تکمیل کرد که نشان می داد بین کاربرد موضعی DEA و برخی از ترکیبات مرتبط با DEA و سرطان در حیوانات آزمایشگاهی ارتباط وجود دارد. برای ترکیبات مربوط به DEA ، مطالعه NTP نشان می دهد که واکنش سرطان زا با سطوح احتمالی باقی مانده DEA مرتبط است. مطالعه NTP ارتباطی بین DEA و خطر سرطان در انسان ایجاد نکرد.
مواد تشکیل دهنده مربوط به DEA و DEA به عنوان امولسیفایر یا عوامل کف کننده در لوازم آرایشی عمل می کنند یا pH محصول (اسیدیته) را تنظیم می کنند. بر اساس اطلاعات ثبت شده در برنامه ثبت نام لوازم آرایشی داوطلبانه FDA ، به نظر می رسد که ترکیبات مربوط به DEA و DEA در محصولات آرایشی بسیار کمتر از زمانی که NTP مطالعه خود را تکمیل کرده است استفاده می شود.
جهت دریافت قیمت و خرید دی اتانول آمین به Bismoot.com مراجه نمایید.
به طور کلی ، به جز اکثر افزودنی های رنگی و آن دسته از موادی که استفاده از آنها در لوازم آرایشی ممنوع یا محدود شده است ، یک تولید کننده می تواند از هر ماده ای در فرمولاسیون یک محصول آرایشی استفاده کند به شرط اینکه مواد اولیه و لوازم آرایشی نهایی ایمن باشند. به درستی برچسب گذاری شده است ، و استفاده از ماده خاص در غیر این صورت باعث تقلب یا علامت گذاری نامناسب بر اساس قوانین FDA نمی شود.
FDA معتقد است که در حال حاضر هیچ دلیلی برای نگرانی مصرف کنندگان بر اساس استفاده از این مواد در لوازم آرایشی وجود ندارد. با این حال ، مصرف کنندگان که مایل به اجتناب از مواد آرایشی حاوی مواد DEA یا DEA هستند ، می توانند با بررسی دستورالعمل مواد تشکیل دهنده که لازم است در برچسب ظروف بیرونی لوازم آرایشی که برای فروش خرده فروشی به مصرف کنندگان ارائه می شود ، ظاهر شوند. موارد زیر برخی از رایج ترین مواد مورد استفاده در DEA هستند:
Cocamide DEA
Cocamide MEA
DEA-Cetyl Phosphate
DEA Oleth-3 فسفات
لاورامید DEA
لینول آمید MEA
میریستامید DEA
Oleamide DEA
استئارامید MEA
TEA-Lauryl Sulfate
تری اتانول آمین
اگر FDA تشخیص دهد که خطری برای سلامتی وجود دارد ، آژانس به صنعت و مردم توصیه می کند و گزینه های قانونی خود را تحت نظارت قانون فدرال مواد غذایی ، دارویی و آرایشی در حفاظت از سلامت و رفاه مصرف کنندگان در نظر می گیرد.
منابع مرتبط
مقامات FDA در زمینه لوازم آرایشی
https://www.fda.gov/cosmetics/cosmetic-ingredients/diethanolamine
سدیم هیدروکسید در کدام محصولات بکار میرود؟ نکات ایمنی سدیم هیدروکسید
هیدروکسید سدیم (NaOH) چیست؟
هیدروکسید سدیم گاهی اوقات سود سوزآور یا لیس نامیده می شود. این یک ماده رایج در پاک کننده ها و صابون ها است.
در دمای اتاق ، هیدروکسید سدیم یک جامد سفید و بی بو است. هیدروکسید سدیم مایع بی رنگ است و فاقد بو است. می تواند با اسیدهای قوی و با آب واکنش شدیدی نشان دهد. هیدروکسید سدیم خورنده است. NaOH می تواند با رطوبت هوا واکنش نشان دهد و ممکن است هنگام حل شدن ، گرما ایجاد کند. اگر در نزدیکی مواد قابل اشتعال باشد ، این گرما می تواند به حدی باشد که باعث آتش سوزی شود.
هیدروکسید سدیم به دلیل توانایی آن در تغییر چربی ها مفید است. از آن برای تهیه صابون و به عنوان عنصر اصلی در محصولات خانگی مانند شوینده های مایع استفاده می شود. هیدروکسید سدیم معمولاً به صورت خالص به صورت گلوله های سفید یا محلول در آب فروخته می شود.
هیدروکسید سدیم چه کاربردهایی دارد؟
از هیدروکسید سدیم در صابون ها و شوینده ها استفاده می شود. هیدروکسید سدیم همچنین به عنوان یک پاک کننده تخلیه برای باز کردن لوله ها استفاده می شود.
حدود 56 درصد از هیدروکسید سدیم تولید شده توسط صنعت و 25 درصد از NaOH در صنعت کاغذ استفاده می شود. برخی کاربردهای دیگر شامل تولید سلول سوختی ، درمان غذا ، برداشتن پوست سبزیجات برای کنسرو ، سفید کننده ، تمیز کننده تخلیه ، تمیز کننده فر ، صابون ، مواد شوینده ، کاغذسازی ، بازیافت کاغذ ، پردازش سنگ آلومینیوم ، پوشش اکسید ، پردازش پارچه پنبه ای ، ترشی ، مسکن ها ، داروهای ضد انعقاد برای جلوگیری از لخته شدن خون ، داروهای کاهش دهنده کلسترول و درمان آب.
چگونه ممکن است در معرض هیدروکسید سدیم قرار بگیرید؟
در خانه ، برخی وسایل خانگی مانند صابون ها یا پاک کننده ها حاوی هیدروکسید سدیم هستند. بلعیدن یا تماس پوستی با این پاک کننده ها می تواند باعث تماس مضر شود.
برخی از محل های کار صنعتی از هیدروکسید سدیم استفاده می کنند. در اینجا برخی از محدودیت های مواجهه محل کار با NaOH در هوا آورده شده است.
محدودیت های قرار گرفتن در معرض هوای محل کار:
OSHA: هوایی قانونی
حد مجاز قرار گرفتن در معرض (PEL) به طور متوسط 2 میلی گرم در متر مکعب در یک شیفت کاری 8 ساعته است
NIOSH: هوابرد توصیه شده
حد قرار گرفتن در معرض (REL) 2 میلی گرم در متر مکعب است که نباید در هر زمان از آن تجاوز کرد
ACGIH: مقدار حد آستانه
(TLV) 2 میلی گرم در متر مکعب است که نباید در هر زمان از آن تجاوز کرد
چگونه می توانید از خانواده خود در برابر تماس محافظت کنید؟
• تمام اقدامات احتیاطی و دستورالعمل های روی برچسب محصول را دنبال کنید.
• محصولات تمیز کننده را دور از دسترس کودکان نگهداری و نگهداری کنید.
• محصولات پاک کننده را در بسته بندی اصلی خود نگهداری کنید.
• هنگام استفاده از محصولات حاوی غلظت بالای NaOH دستکش لاتکس یا نیتریل بپوشید.
• برای محافظت از پوست خود ، آستین بلند و شلواری بپوشید که با سدیم هیدروکسید قابل تخریب یا خراب شدن نباشد. لباس ها را در صورت خیس شدن با دقت بیرون آورید تا از پخش شدن سدیم هیدروکسید بر روی پوست خود جلوگیری کنید.
قرار گرفتن در معرض هیدروکسید سدیم چه اثرات مضر بالقوه ای دارد؟
هیدروکسید سدیم یک ماده بالقوه خطرناک است. اگر پوست شما را لمس کند ، آن را بنوشید یا اگر تنفس کنید می تواند به شما آسیب برساند. خوردن یا نوشیدن هیدروکسید سدیم می تواند باعث سوختگی شدید و استفراغ فوری ، حالت تهوع ، اسهال یا درد قفسه سینه و معده و همچنین مشکل بلع شود. آسیب به دهان ، گلو و معده فوری است. تنفس آن می تواند باعث تحریک شدید دستگاه تنفسی فوقانی با سرفه ، سوختگی و مشکل در تنفس شود.
اثرات مضر هیدروکسید سدیم به عوامل مختلفی بستگی دارد از جمله غلظت هیدروکسید سدیم ، مدت زمان قرار گرفتن در معرض آن ، و اینکه آیا شما آن را لمس کرده اید ، نوشیدید یا استنشاق کرده اید. تماس با غلظت های بسیار زیاد هیدروکسید سدیم می تواند باعث سوختگی شدید در چشم ها ، پوست ، دستگاه گوارش یا ریه ها شود که منجر به آسیب دائمی یا مرگ می شود. تماس طولانی مدت یا مکرر با پوست ممکن است باعث ایجاد درماتیت شود. استنشاق مکرر بخار هیدروکسید سدیم می تواند منجر به آسیب دائمی ریه شود.
کمک های اولیه
در مواقع ضروری با 911 تماس بگیرید.
ارتباط چشمی
چشم ها را به مدت 30 دقیقه با آب بشویید.
پلک های بالا و پایین را بلند کنید.
لنزهای تماسی را بردارید.
تماس پوستی
لباسهای آلوده را بردارید.
به مدت 15 دقیقه با آب شستشو دهید.
استنشاق
در صورتی که انجام این کار برای شما بی خطر است ، فرد را از تماس دور کنید.
اگر فردی واکنش نشان نمی دهد و به طور معمول تنفس نمی کند ، CPR را شروع کنید.
گوارشی
از استفراغ شخص خودداری کنید.
هرگز چیزی را از طریق دهان به یک فرد بیهوش ندهید.
اگر فرد کاملاً هوشیار است و از ناراحتی تنفسی رنج نمی برد ، یک فنجان آب به او بدهید تا هیدروکسید سدیم رقیق شود.
برای کسب اطلاعات بیشتر در مورد قرار گرفتن در معرض هیدروکسید سدیم ، با مرکز سم به شماره 1-800-222-1222 تماس بگیرید.
حوادث هیدروکسید سدیم در تنسی
در سال 2010-2011 ، هیدروکسید سدیم به عنوان یکی از 10 ماده شیمیایی رایج در تنسی منتشر شده بود. حدود 50 درصد از این نشت و انتشار در انبارها یا در حین حمل و نقل رخ داده است. حدود 75 درصد آنها به دلیل خطای انسانی بوده است.
حمل و نقل و انبار
نشت و شرایط اضطراری - اگر کارکنان ملزم به پاکسازی نشت ها هستند ، باید به درستی آموزش دیده و تجهیز شوند. ممکن است عملیات زباله های خطرناک OSHA و استاندارد واکنش اضطراری (29 CFR 1910.120) اعمال شود.
در صورت ریختن یا نشت هیدروکسید سدیم ، مراحل زیر را انجام دهید:
پرسنل را تخلیه کرده و ورودی آن را ایمن و کنترل کنیدحوزه.
تمام منابع احتراق را حذف کنید.
برای هیدروکسید سدیم در محلول ، مایعات را در ماسه خشک ، خاک یا یک ماده مشابه جذب کنید و برای دفع در ظروف مهر و موم شده قرار دهید.
مواد جامد را به راحت ترین و ایمن ترین حالت جمع آوری کرده و برای دفع در ظروف مهر و موم شده قرار دهید.
برای پاکسازی NaOH از آب آب یا هر روش مرطوب استفاده نکنید.
پس از اتمام پاکسازی ، منطقه را تهویه و بشویید.
در فاضلاب شستشو نشود.
ممکن است لازم باشد که سدیم هیدروکسید را به عنوان یک ضایعات خطرناک دفع کنید.
هیدروکسید سدیم با اسیدهای قوی (هیدروکلریک ، سولفوریک یا نیتریک) ، آب و رطوبت واکنش می دهد و به سرعت گرما را آزاد می کند.
هیدروکسید سدیم با فلزات (آلومینیوم ، سرب ، قلع یا روی) واکنش داده و گاز هیدروژن قابل اشتعال و انفجاری ایجاد می کند.
هیدروکسید سدیم در تماس با ترکیبات حاوی نیتروژن می تواند نمک های حساس به ضربه ایجاد کند.
هیدروکسید سدیم با عوامل اکسید کننده ، حلالهای کلر دار ، آمونیاک و مواد آلی سازگار نیست.
در ظروف اصلی ، محکم بسته ، در محفظه ای خنک و با تهویه مناسب و دور از آب و رطوبت نگهداری شود.
هیدروکسید سدیم می تواند به آهن ، مس ، پلاستیک ، لاستیک و روکش ها حمله کند.
منبع
https://www.tn.gov/health/cedep/environmental/environmental-health-topics/eht/sodium-hydroxide.html
کاربرد اسید فسفریک مایع خانگی+ خرید اسید فسفریک
کاربرد اسید فسفریک مایع خانگی
کاربرد اسید فسفریک مایع
پس از نیتروژن (N) ، فسفر (P) دومین ماده مغذی گیاهی است که به طور گسترده ای در خاک های نرمال (82 - 90٪) و خاک های تحت تاثیر نمک (93٪) پنجاب کمبود دارد. این گیاه تقاضا پر شده است از طریق لقاح اما بهره وری (بازیابی توسط گیاه) از هیچ یک از موجود کودهای اعمال شده از طریق پخش بیش از 20 % با توجه به اجتناب ناپذیر واکنش های شیمیایی در خاک آهکی قلیایی بیماری است که تبدیل به یک شیر به اشتراک گذاری (80 %) از اعمال P به شکل غیر قابل دسترس برای گیاه است. بهره.پایین تر از کود P موجود خواستار افزایش استفاده از آنها که در حال تبدیل شدن عملا دشوار با توجه به افزایش قیمت در حال حاضر در کود P و خروج یارانه. قیمت های بالاتر کود فسفات به کاربردهای بسیار کم P به محصولات منعکس می شود و منجر به کاهش شدید عملکرد محصولات کشاورزی در آینده نزدیک می شود. این وضعیت در حال حاضر زمان برای پاسخگویی به تقاضای توده ها برای مواد غذایی به خصوص غلات و حبوبات را تشدید کند. این سناریو می توانید با موجود گران نمی شود/ منابع P ناکارآمد (کود مشترک) و روش های کاربردی. معمولا با استفاده از روش پخش قبل از کاشت بی فایده است به عنوان آن را تا حد زیادی محدودیت سودمندی P کود با توجه به قرار گرفتن در معرض آن به سطح خاک منطقه که در آن حداکثر P تثبیت می گیرد قبل از آن گرفته شده است تا این محصول است. با این حال ، باندهای حاصل از کود P از طریق یک مته بذر تقدیر کود می تواند 70 ٪ از کود که در کاهش بزرگ در هزینه های وارده بر واردات آنها منجر خواهد شد را نجات دهد.
مراکش و تونس صادرکنندگان بزرگ کود فسفات هستند و همچنین علاوه بر کودهای فسفات ، اسید فسفریک کشاورزی (سبز) را نیز صادر می کنند. آمونیزه کردن مواد خام (اسید فسفریک) برای تولید dap هزینه تولید را افزایش می دهد. با این حال ، استفاده مستقیم از اسید فسفریک قطعا مقرون به صرفه تر خواهد بود زیرا پردازش بیشتر را حذف می کند.
خواص اسید فسفریک موجب ایجاد کاربردهای فراوانی برای آن شده است.
علاوه بر این ، این امر می تواند در بهبود ساختار خاک ما که آهکی قلیایی در طبیعت مفید است. مطالعات قبلی نشان داده است که استفاده از اسید فسفریک CaCO3 و MgCO3 در خاک آزاد Ca++ و Mg++حل شده است. این کاتیونها به احتمال زیاد با PO4 از اسید واکنش نشان دادند تا فسفات Ca و mg کمی محلول ایجاد کنند که به عنوان عامل سیمان در دانه های خاک عمل می کنند. در این مطالعات همچنین مشاهده شد که کاربرد اسید فسفریک سبب بهبود ظهور نهال چغندر قند شده است. همچنین اثر اسید فسفریک بر پایداری کل با استفاده از تکنیک جدید توسعه یافته توسط دانشمند نیاب برای تعیین پایداری ساختاری خاک مورد ارزیابی قرار گرفت. نتایج نشان داد که افزودن اسید فسفریک بر ثبات کل خاک تاثیر نمی گذارد. اثر اسید فسفریک بالا بر ماده آلی در خاک مورد بررسی قرار گرفت. هیچ اثر نامطلوب کاربرد اسید فسفریک بر محتوای مواد آلی خاک مشاهده نشد. در یک آزمایش جوانه زنی در گلخانه ای در نیاب انجام, مشاهده شد که قرار دادن باند از درجه کشاورزی اسید فسفریک کاملا نزدیک به دانه جوانه زنی دانه گندم تاثیر نمی گذارد.
هدف
شناسایی جایگزین های ارزان تر و کارآمد کود فسفات تجاری برای کمک به کشاورزان برای حفظ برنامه های کاربردی کود متعادل برای حفظ بهره higher محصول بالاتر
طرح پروژه
توسعه و ارزیابی قرار دادن باند مته بذر-تقدیر مایع کود اپلیکاتور برای گندم
توسعه و ارزیابی قرار دادن باند بذر زمینی-تقدیر مایع کود اپلیکاتور برای ذرت
منبع